Цель урока - формирование ключевых знаний у учащихся об изомерии, гомологии, строении, свойствах, способах получения, применения алканов
- ознакомить учащихся с изомерией предельных УВ, их физическими и химическими свойствами и основными способами получения.
- показать единство материального мира на примере генетической связи углеводородов разных гомологических рядов, получаемых при переработки природного и попутного нефтяного газов, нефти и каменного угля.
- способствовать развитию коммуникативной культуры (умение работать в паре и группе), воспитывать аккуратность учащихся при выполнении и оформлении записей в тетради.
Педагогические технологии, используемые на уроке: информационные, групповые, проблемные, критического мышления.
· Познавательные УУД: поиск и выделение необходимой информации; применение методов информационного поиска; смысловое чтение; понимание и адекватная оценка языка средств массовой информации;
Развитие умения работать с текстом учебника, с дополнительными источниками информации, анализировать, отбирать и представлять необходимую информацию;
· Регулятивные УУД: умение определять цели, ставить задачи на каждом этапе урока.
· Коммуникативные УУД: развитие навыков коммуникативной культуры и сотрудничества при работе в группах; коллективной работе, воспитание информационной компетентности.
· Личностные: смыслообразование - установление учащимися связи между целью учебной деятельности и ее мотивом.
Тип урока: урок изучения нового материала.
Демонстрационный материал: компьютер, мультимедиа проектор, экран, презентация, шаростержневые модели молекул, географическая карта полезных ископаемых России. Текст по природному газу и вопросы для групп.
| Этап урока | Деятельность учителя. | Деятельность учащихся | примеч |
| 1.Организационный момент урока. 1.1. Постановка задач. | Организация внимания и порядка в классе, взаимное приветствие, проверка присутствующих, проверка готовности класса к уроку. | Готовятся к уроку, приветствуют учителя. |
|
Организация проверки изученного на прошлом уроке материала.
| Самостоятельная работа. | Выполняют работу и сдают на проверку. |
|
| 2. Изучение новой темы.
| Актуализация знаний проходит через обсуждение проблемной ситуации и решение расчётной задачи, ответом в которой является метан – горючий газ, алкан. «Не так давно случилась на Кольском полуострове небывалая история. Горный инженер, работавший в апатитовом руднике близ города Кировска, услышал какой-то странный свист и шум, идущий из-под земли. Кто-то из рабочих неосторожно предложил: «Попробуем – подожжем?..» И попробовали... Вспыхнувшая спичка вызвала взрыв. К счастью, инженер и рабочие отделались только ожогами. Позднее выбросы газа повторились. Химики определили, что в состав газа входит 75 % углерода и 25 % водород, относительная плотность газа по воздуху равна 0,55. Что за газ чуть не унес жизни людей?» После получения ответа учитель формирует тему урока совместно с учащимися и определяют план изучения класса органического соединения.
| Решают расчетную задачу. После объявления темы урока и плана изучения, пробуют сформулировать цель урока и план изучения класса соединения. | Слайд 1-3 |
| 2.1. Нахождение веществ в природе и их значении в жизни человека | Учитель сообщает ученикам о нахождении этих веществ в природе На этапе происходит представление сообщений (мультимедийных презентаций), подготовленных учащимися самостоятельно в малых группах Лабораторный опыт: Знакомство с образцами природных УВ и продуктами их переработки (работа с коллекциями) | Составляют опорный конспект и записывают его в тетрадь. Сообщения учащихся: «Алканы в природе», «Применение алканов», «Двойственная роль метана в биосфере» Работа с коллекциями | Слайд 4-10
|
| 2.2. Определение класса алканы, общая формула, гомологический ряд алканов | Организует беседу по вопросам - Давайте вспомним классификацию органических соединений в зависимости от строения углеродной цепи и дадим определение классу алканы! - Куда же относятся в этой классификации алканы? -Из каких атомов состоят молекулы этих соединений, о чем это говорит? - О чем свидетельствует наличие суффикса -ан ? Так какое же определение мы можем с вами дать этому классу соединений? -Давайте вспомним общую формулу данного класса, раз они являются насышенными углеводородами? На доске, основываясь на общую формулу, учитель записывает вместе с учениками гомологический ряд алканов. | - В зависимости от строения углеродной цепи органические соединения разделяют на соединения с открытой цепью 1) ациклические (алифатические) и 2) циклические — с замкнутой цепью атомов. - К ациклическим соединеням -Из атомов С и Н, о том, что данные соединения являются углеводородами - О том, что между атомами углерода только одинарные (-связи) -Алканы - это ациклические углеводороды, в молекулах которых между атомами углерода содержатся только одинарные связи -СnH2n+2 Записывают определение, общую формулу, гомологический ряд
| Слайд 11-12 |
| 2.3.Изомерия | Лабораторный опыт: «Изготовление моделей молекул алканов» При составлении модели бутана у учащихся должно получиться 2 модели: n- бутан и изобутан(2-метилпропан). -Давайте вспомним как называются вещества с одинаковой молекулярной формулой(состав тот же), но строение разное? - Какой же вид изомерии характерен для класса алканы?
| Выполняют лабораторный опыт.
-Изомеры; -Изомерия углеродного скелета(цепи)
| Слайд 13-14 |
| 2.4.Номенклатура алканов.
| -Давайте вспомним правила образования названий органических веществ по международной номенклатуре (ИЮПАК), а именно для алканов. На доске записывается структурные формулы разветвленных алканов (2 структуры). -Сейчас по очереди 2 студента будут выходить к доске и дописывать недостающие атомы водорода в соединениях, а также дадут названия этим соединениям. -А теперь следующие 2 студента, зная названия соединений должны будут написать структурные формулы этих веществ. | -Находим в первую очередь самую длинную углеродную цепочку, затем нумеруем ее (количество атомов углерода главной цепи-это и есть название основы(корня)) таким образом, чтобы заместители получили наименьшие цифры(они записываются в виде приставки, указываются также их положения цифрами, если одинаковых заместителей несколько, то после цифр, перед названием самих радикалов, появляются приставки ди-(2),три-(3),тетра-(4) и т.д.).Наличие одинарных связей между атомами углерода главной цепи обозначают суффиксом –ан, после корня. -Выходят к доске, дописывают недостающие атомы водорода и указывают названия. -Выходят к доске и записывают структурные формулы, зная названия. | Слайд 15 Слайд
|
| 2.5.Физические свойства алканов
| Работа с учебником, учащиеся должны найти в учебнике информацию про агрегатное состояние, растворимость в воде и других растворителях, зависимость Ткип и Тпл от значения Mr;
| Работа с учебником, записывают в тетрадь. | Слайд 16 |
| 2.6. Строение алканов. | -Какой тип гибридизации характерен для каждого атома углерода в молекулах алкана? как еще называют данный тип гибридизации? -Как образуется данный тип гибридизации, для этого вспомните основное и возбужденное состояния атомов углерода? -Чему равен валентный угол между 4 sp3-гибридными орбиталями? Установить причинно-следственную связь между строением и химическими свойствами алканов. Выявить типы реакций, характерные для алканов , и условия их протекания. -Так какие же типы реакций характерны для алканов? | -sp3-гибридизация(тетраэдрическая) -электронная конфигурация в основном состоянии на внешней орбитали-2s22p2; в возбужденном состоянии-2s12p3, атом С в органических соединениях находится в возбужденном состоянии, sp3-гибридизация образуется путем смешивания одной s- и три р-орбитали,в ходе чего и образуются четыре равноценные по форме и энергии sp3-гибридные орбитали. -Валентный угол=10928 Заполняют таблицу -Для алканов характерны следующие типы химических реакций:
| Слайд 17-20
Слайд 21-22 |
| 2.7.Химические свойства | Давайте остановимся на каждом типе реакций более подробно. 1) Замещение атомов водорода: А) реакция галогенирования: CH4 +Cl2 → CH3Cl + HCl. Вспоминают про радикальный механизм, который рассмотрел впервые Семенов Н.Н. Б) реакция нитрования (Коновалова): C4H10+HO-NO2---C4H9NO2+H2O. В) реакция сульфирования: CH4 + HО-SO3Н → CH3-SO3 H + H2O + Q 3) Реакция с водяным паром: CH4 + H2O→ CO + 3H2 4) Реакция дегидрирования: 2СН4 → НС=СН + 3Н2 + Q 5) Реакция окисления: CH4 + 2O2 → Н-C + 2H2O + Q 6) Горение метана: CH4 + 2O2 → CO2 + 2H2O + Q Демонстрация опыта: «Горение твердых и жидких алканов» (видеоопытом.)
| Выходят к доске по одному для записи реакций, также оформляют в тетради эти записи | Слайд 23-40 |
| 2.8.Способы получения алканов | 1.Выделение УВ из природного сырья 2.Разложение карбидов металлов (метанидов) водой:  3.Декарбоксилирование солей карбоновых кислот 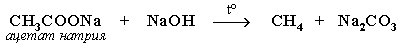 4. Синтез более сложных алканов из галогенопpоизводных с меньшим числом атомов углеpода:
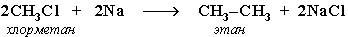 (реакция Вюpца)
| Записывают эти реакции в тетради. | Слайд 41-44 |
| 3. Закрепление материала. | Зачитывает задания со слайдов. | Работают в тетради, отвечают на вопросы учителя. | Слайд 45-53
|
| 4. Рефлексия | Игра «Что я за птица?» | критерий
| 3 балла | 2 балла | 1 балл | | Активность на уроке
| высокая | средняя | низкая | | Материал урока усвоил | хорошо | частично | слабо | | Тему могу объяснить | Могу сам | Могу, но с подсказкой | Затрудняюсь |
|
3-5 баллов воробей (собирает знания по крупицам) 7-6 баллов Соловей (поведай свои знания другим) 8-9 баллов Орел (открывает тайны бытия) | Слайд 54 |
| 5. Дом. задание | Параграф___ ,задания |
| Слайд 55 |




















